 18年一站式净化厂房解决方案供应商
18年一站式净化厂房解决方案供应商
服务热线:
020-84211735
13902406190
原料药洁净室设计规范的核心在于融合GMP合规性、防爆安全与污染控制,确保在高风险化学工艺下实现药品质量与生产安全的双重保障。
一、GMP合规性:贯穿全生命周期的质量基础
GMP(药品生产质量管理规范)要求洁净室设计从源头控制质量风险,强调“质量源于设计” 。关键点包括:
人、物流分离:严格划分人员进出通道与物料运输路径,避免交叉污染。设置更衣间、缓冲间和传递窗等设施,实现气闸隔离 。
功能区合理布局:按工艺流程划分原料存储、生产、包装等功能区,洁净区与非洁净区明确分隔,质检实验室与生产区物理隔离 。
文件与验证体系:所有设计参数需有文件支持,并通过安装确认(IQ)、运行确认(
OQ)和性能确认( PQ)完成验证,确保可追溯 。
二、防爆安全:应对甲类厂房的特殊挑战
原料药生产常涉及易燃易爆溶剂,多数区域属甲类防爆区,设计必须符合《建筑设计防火规范》与化工安全标准:
设备防爆等级:关键区域设备需满足Ex d IIB T6或更高防爆等级;加氢反应区则需
CT4以上 。
电气与暖通系统:照明、风机、传感器等均需防爆认证;空调系统送排风阀应具备防爆功能,排风系统独立设置并经净化处理后排放 。
结构与材料:墙体采用玻镁彩钢板,接缝密封处理;地面为防静电PVC材质,防止火花积聚 。
三、污染与交叉污染控制:三重屏障策略
为防止微粒、微生物及产品间交叉污染,采用“物理隔离+气流控制 +操作管理”三位一体机制:
物理屏障:高致敏类(如青霉素)或高活性物质生产区必须独立建制,配备专用空气净化系统,与其他区域严格分开 。
气流组织:
洁净区维持正压(≥10Pa),防止外部污染物侵入;
粉尘产生区(如称量、粉碎)设局部负压,配合下侧回风快速捕获颗粒 。
清洁与消毒:墙面与地面交界处设计为弧形,减少积尘死角;定期执行臭氧、紫外线或化学试剂消毒程序 。
四、洁净等级匹配:按工艺需求分级控制
根据《医药工业洁净厂房设计规范》(GB50457-2019)及ISO 14644 标准,洁净室划分为不同等级:
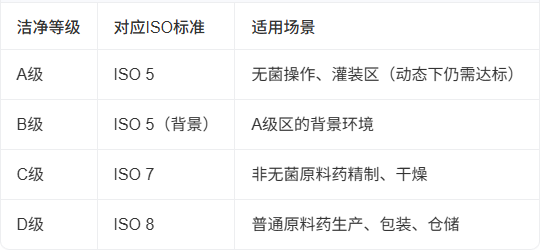
注:原料药车间以C、D级为主,仅在无菌分装等特殊环节提升至
A/B 级 。温湿度通常控制在18~26
℃、45%~ 65%RH,露点可低至
-40℃以下以适应特殊工艺 。